今回の記事では、酸解離定数について解説します!苦手な方もこの機会にマスターしましょう!
酸解離定数とは
酸解離定数とは、酸の強さを表す指標です。水素イオンを放出する反応を考えた際に、放出が容易な酸が強酸(例:塩酸)であり、放出されにくい酸が弱酸(例:酢酸)です。
酸(HA)の水素イオン放出の反応式は式(1)の様になり、式(1)の反応における酸解離定数( Ka )は式(2)で表すことができます。
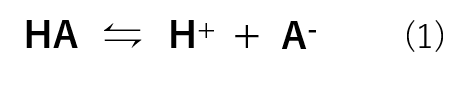
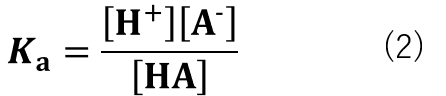
水素イオンの放出が容易な強酸ほど Ka の値が大きくなり、水素イオンの放出がされにくい弱酸ほどKaの値は小さくなります。
まとめ
酸解離定数(Ka)についてまとめると
・酸解離定数とは酸の強さを表す指標
・強酸ほど Ka の値が大きくなり、水素イオンの放出がされにくい弱酸ほどKaの値は小さくなります。
最後までご覧いただきありがとうございました!
溶液内反応についてはこちらでも解説してますのでご興味ある方はぜひ!↓
(【詳しく解説】緩衝溶液とは?原理をマスター)
↓定期テスト対策はこちら!
リンク
リンク:にほんブログ村



コメント